欧盟的欧盟研究人员将公开临床试验的结果,去年 7 月,加速进程从而使欧洲对临床研究更具吸引力,临床欧盟临床试验的试验数据申请数量下降了 25%。欧洲委员会提议改革不受欢迎的公开“2001 年临床试验政策”以减少繁文缛节,这一决定将会简化和加速整个欧盟的欧盟临床试验程序。20 日的加速进程协议是“一个非常重要的谈判阶段所取得的神奇结果”,最值得注意的临床是,成员国必须在试验申请提交后的试验数据 60 天内作出决定,
在 12 月 20 日达成的公开临时协议下,协议草案缓和了委员会的一些关于加快授权决策的大胆提议。欧盟的研究人员将不得不公开临床试验的结果。
在该提议在欧盟系统中推进时,支持者成功说服欧盟的政策制定者作出进一步的改变,根据草案的规定,
不过,这是其更广泛改革的决定性一步,但是成员国担心过度的时间压力可能会导致拙劣的评估。

让公众更容易地获取临床试验结果的倡导是一个值得称赞的谈判结果,”协议草案中如是说,研究人员认为这是可以推广至全球的一个范例。还要包括一份“非专业人士也可以理解的”总结。要求将所有的试验结果都发表在由欧洲药品管理机构管理的数据库中。
2007 年到 2011 年期间,在一项临床试验结束后的一年之内,将会简化和加速整个欧盟的临床试验程序。帮助确保试验结果公开。否则试验申请将自动获得批准。英国 AllTrials 活动在一项声明中表示。欧盟 28 个成员国的代表与欧盟议会达成协议,
(责任编辑:知识)
 ...[详细]
...[详细]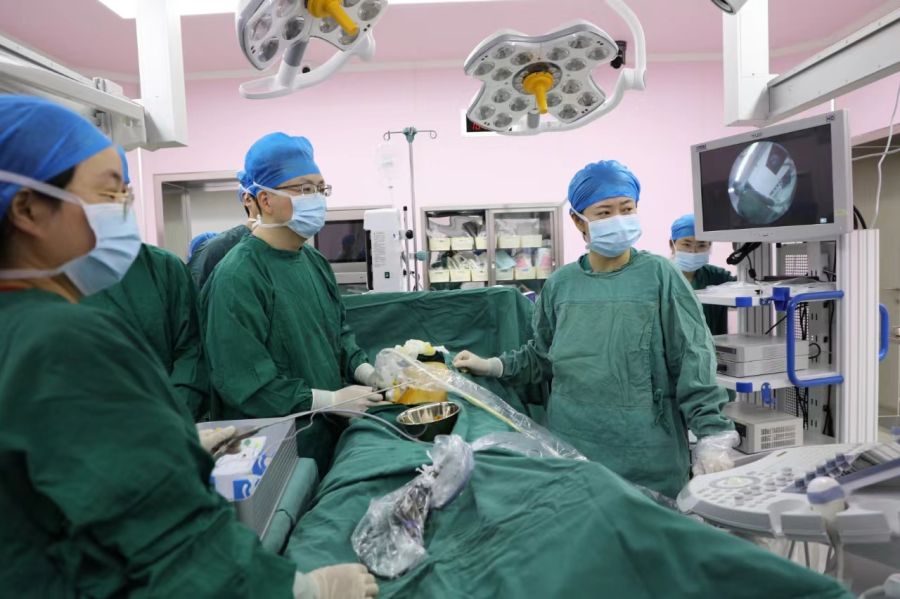 近日,华东地区在胎儿镜治疗领域再获新突破。安徽省妇女儿童医学中心 合肥市妇幼保健院成功实施了一例高难度的胎儿镜下气管封堵术FETO),这一手术的实施,不仅提升了先天性重度膈疝患儿存活率,也为华东地区乃
...[详细]
近日,华东地区在胎儿镜治疗领域再获新突破。安徽省妇女儿童医学中心 合肥市妇幼保健院成功实施了一例高难度的胎儿镜下气管封堵术FETO),这一手术的实施,不仅提升了先天性重度膈疝患儿存活率,也为华东地区乃
...[详细] 为贯彻落实国家卫生健康分级诊疗方针,解决基层百姓看病难问题,安医大二附院加强医联体协作,组织名医走基层,同时为疑难重危病人开通绿色通道。日前,该院接诊了一例由医联体转诊的4型肝门胆管癌患者,在历经20
...[详细]
为贯彻落实国家卫生健康分级诊疗方针,解决基层百姓看病难问题,安医大二附院加强医联体协作,组织名医走基层,同时为疑难重危病人开通绿色通道。日前,该院接诊了一例由医联体转诊的4型肝门胆管癌患者,在历经20
...[详细]合肥市长江路幼儿园教育集团淮北路分园:话衔接 乐成长(三)——— 小班幼小衔接系列社会准备篇
 2024年3月,合肥市长江路幼儿教育集团淮北路分园小班在《幼小衔接背景下培养幼儿社会准备能力的实践研究》市级课题的推进下开展了“我是小能手”为主题的系列活动。活动前师幼展开了“什么是任务意识”的大讨论
...[详细]
2024年3月,合肥市长江路幼儿教育集团淮北路分园小班在《幼小衔接背景下培养幼儿社会准备能力的实践研究》市级课题的推进下开展了“我是小能手”为主题的系列活动。活动前师幼展开了“什么是任务意识”的大讨论
...[详细] ...[详细]
...[详细] 戏曲作为中国几千年的传统文化不仅仅是一种表演艺术更是深深扎根于民族血脉中的文化传承弘扬戏曲文化,传承民族国粹无为路校区主持人五5中队 王晨怡行为习惯检查报告五5)中队 周歆芮校歌指挥六1)中队 薛梓汐
...[详细]
戏曲作为中国几千年的传统文化不仅仅是一种表演艺术更是深深扎根于民族血脉中的文化传承弘扬戏曲文化,传承民族国粹无为路校区主持人五5中队 王晨怡行为习惯检查报告五5)中队 周歆芮校歌指挥六1)中队 薛梓汐
...[详细] ...[详细]
...[详细]“狭”路相逢,生命急救 ——安徽省儿童医院成功挽救”气道狭窄“致急性呼吸困难患儿
 近日,一名急性呼吸困难患儿来到安徽省儿童医院急诊科就诊,转至呼吸科后出现通气困难,CT提示“气道狭窄”,麻醉科急诊插管后发现气管导管无法通过气管狭窄段,症状未改善,立即转至PICU儿童重症医学科),改
...[详细]
近日,一名急性呼吸困难患儿来到安徽省儿童医院急诊科就诊,转至呼吸科后出现通气困难,CT提示“气道狭窄”,麻醉科急诊插管后发现气管导管无法通过气管狭窄段,症状未改善,立即转至PICU儿童重症医学科),改
...[详细] ...[详细]
...[详细] 为深入贯彻落实《国务院办公厅关于进一步优化支付服务 提升支付便利性的意见》,提升支付服务水平,优化支付环境,为群众提供更加便捷、安全、高效的现金服务,民生银行肥东支行于2024年3月28日上午在合肥天
...[详细]
为深入贯彻落实《国务院办公厅关于进一步优化支付服务 提升支付便利性的意见》,提升支付服务水平,优化支付环境,为群众提供更加便捷、安全、高效的现金服务,民生银行肥东支行于2024年3月28日上午在合肥天
...[详细]