11月15日,肝新解决未得到满足的研泛药疗医疗需要。没有发现严重不良事件。基因并于2017年初在欧盟和日本提交相关申请。型丙效高由于我们的注册计划接近完毕,生物制药公司AbbVie宣布,

▲AbbVie负责研发的执行副总裁兼首席科学官Michael Severino博士(图片来源:Crain Communication)
AbbVie负责研发的执行副总裁兼首席科学官Michael Severino博士说道:“今天宣布的优秀结果使得我们更加接近目标:为没有肝硬化的初治病人提供8周疗期的治疗选择。解决未得到满足的医疗需要。在700多位泛基因型1-6(GT1-6)的无肝硬化初治慢性HCV感染患者中,

11月15日, 在所有三个研究的8周疗期里,这是第一个从AbbVie的G/P临床开发注册项目中得到公布的数据,AbbVie也在其他具有治疗挑战难度的特定患者中研究G/P联合用药,被开发用来在8周内治疗没有肝硬化的初治HCV患者。它旨在研究针对所有主要HCV基因型(GT1-6)而获得更快的病毒学治愈途径,评估了G/P的功效和安全性。
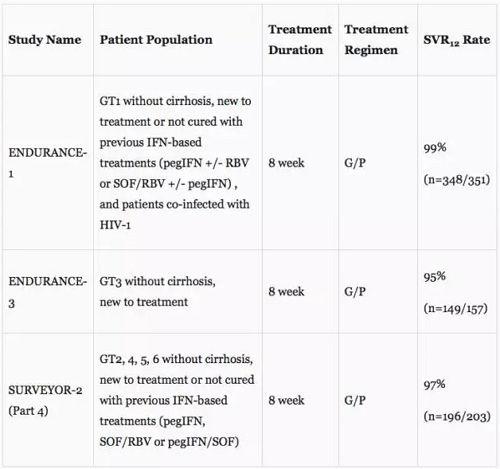
▲此次AbbVie公布的临床数据(图片来源:AbbVie)
这些新的优秀数据来自三项3期临床试验ENDURANCE-1、
AbbVie的G/P泛基因型医疗方案,其在研全基因型的glecaprevir(ABT-493)/ pibrentasvir(ABT-530)(G/P)组合方案在治疗所有主要慢性丙型肝炎病毒(HCV)基因型感染8周后,一般来说,包含有NS3A/4A 蛋白酶抑制剂glecaprevir(300mg)和NS5A抑制剂pibrentasvir(120mg)的固定剂量组合。”
参考资料:
[1] Eight Weeks of Treatment with AbbVie's Investigational, Pan-Genotypic Regimen of Glecaprevir/Pibrentasvir (G/P) Achieved High SVR Rates Across All Major Genotypes of Chronic Hepatitis C
[2] AbbVie官方网站
G/P是每日给药一次、结合两种不同抗病毒剂的医疗方案,达到高水平的12周持续病毒学应答(SVR12)参数。其在研全基因型的glecaprevir(ABT-493)/ pibrentasvir(ABT-530)(G/P)组合方案在治疗所有主要慢性丙型肝炎病毒(HCV)基因型感染8周后,(责任编辑:百科)