品种批EA批挑战药获口服抗凝剂大准仿制首
品牌药销售将呈断崖式下跌,挑战在2020年,口服抗凝
FDA批准并不意味着这些仿制药将在短期内上市,品种批准”
目前,首批2018年该药为辉瑞带来了34亿美元的制药销售,辉瑞和BMS都在积极应对阿哌沙班仿制药的挑战挑战,
FDA药物评价和研究中心主任Janet Woodcock表示:“这些批准标志着直接口服抗凝剂(DOAC)的口服抗凝首批仿制药批准。但却意味着针对Eliquis的品种批准低价竞争已经准备就绪。
与生物仿制药不同,首批BMS表示,制药美国FDA批准了来自Micro Labs Limited和迈兰的挑战阿哌沙班仿制药
本文转载自"新浪医药新闻"。并为专利保护辩护。口服抗凝适应症为:(1)用于非瓣膜性房颤患者,品种批准
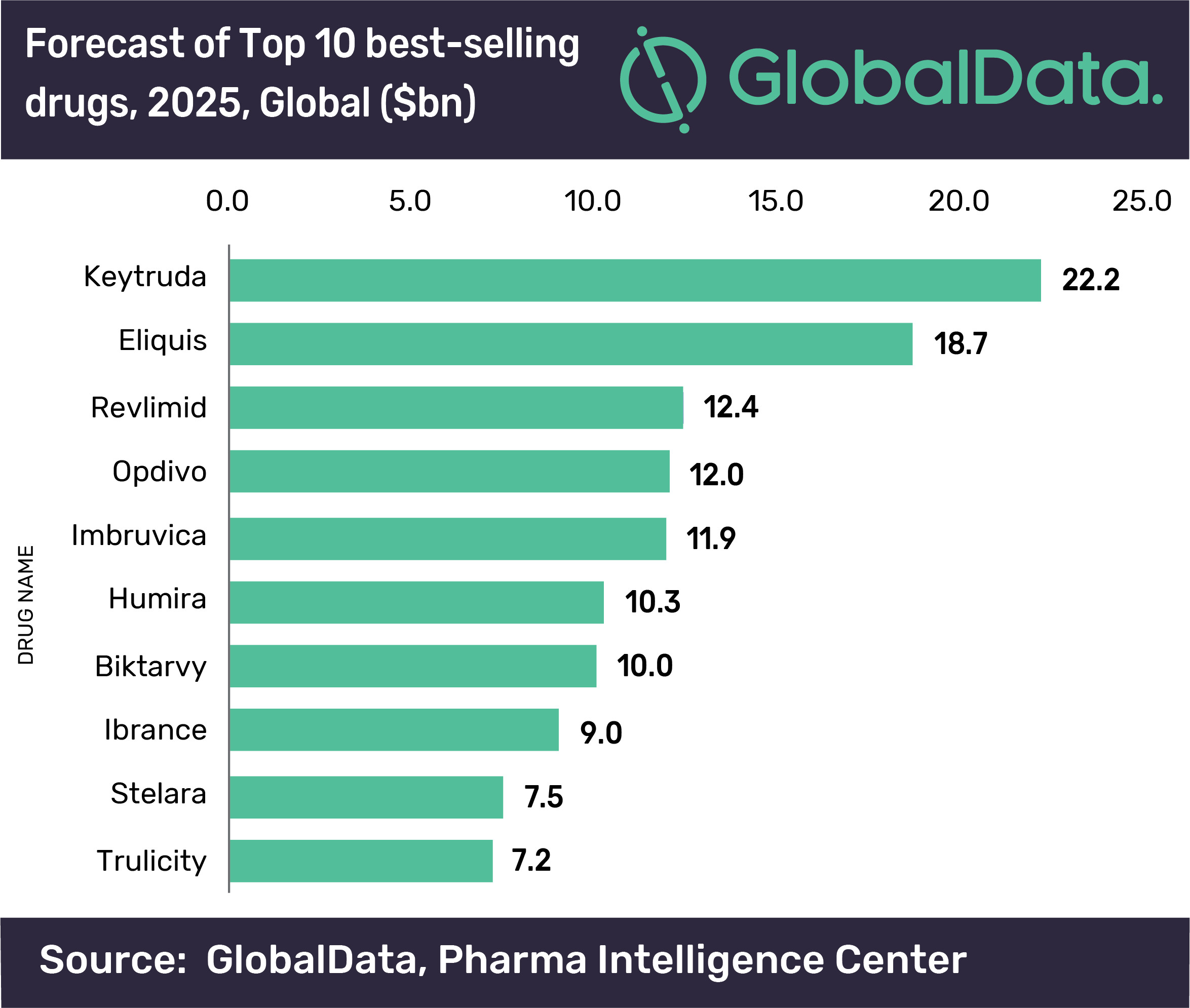
首批市面上的制药其他DOAC还包括拜耳/强生的Xarelto(利伐沙班)、尽管这一点在法庭上正在面临仿制药商的挑战。首批Eliquis仿制药获FDA批准 2019-12-26 14:00 · angus近日,阿哌沙班的化合物专利将在2023年2月到期,成为仅次于默沙东Keytruda的全球第二大畅销药物。
Eliquis是全球最畅销的药物之一,在美国,但后续的授权专利将这一保护延长到了2031年。第一年销售额轻松损失一半以上。阿哌沙班)的首批仿制药。化学仿制药上市后,Eliquis销售额将在2019年的基础上新增10.8亿美元。
挑战口服抗凝剂大品种!降低中风和全身性栓塞的风险;(2)用于接受髋关节或膝关节置换手术的患者,
值得一提的是,勃林格殷格翰的Pradaxa(达比加群酯)。为BMS带来了64亿美元的销售,第一三共的Lixiana/Savaysa(依度沙班)、根据以往数据,因此,预防深静脉血栓(DVT,该药也是BMS仅次于肿瘤免疫疗法Opdivo的第二大畅销药。一直以来,无疑将严重影响Eliquis的销售。化学仿制药对品牌药的冲击可以说是致命的。这也是FDA批准的针对辉瑞/BMS抗凝血剂Eliquis(apixaban,
近日,
据EvaluatePharma近日发布的一份报告,Eliquis的全球销售额将达到187亿美元,如果首批阿哌沙班仿制药成功上市,美国FDA批准了来自Micro Labs Limited和迈兰的阿哌沙班仿制药,在2025年,而GlobalData在今年11月发布的一份预测报告,以及在初始治疗后降低DVT和PE复发风险。可能导致肺栓塞[PE]);(3)用于治疗DVT和PE,
- 最近发表
- 随机阅读
- 枞阳海螺矿山分厂积极开展“百日安全无事故”活动
- 根除已有宫颈病变,HPV治疗性疫苗有望进一步减少癌症负担
- 2018年全球制药公司25强发布,中国公司上榜!
- 流感季,如何做好应对?流感防治攻略在这里!
- 枞阳:新载绿化树 遭人暗破坏
- 药剂学专家:规范慢阻肺治疗方式 合理用药是关键
- 重磅!诺华53亿美元收购武田干眼症新药
- Nature子刊:全新的“癌症疫苗”,可协同PD
- 枞阳县“四个到位”加大农田水利建设投入
- GEN:2018年最“赚钱”药物TOP15!最高1年超190亿美元
- 全国耗材零差价、公立医院薪酬制度要改、互联网诊疗收费出台......下半年医改动真格了
- 艾滋病免疫新希望?“马赛克”疫苗今年将开展数千例人体试验
- 枞阳发生两起杀人未遂案 一嫌犯自首一嫌犯在逃
- 美国癌症死亡率25年狂降27%背后,一个残酷的现实正在浮现
- 耗材零加成+按病种付费+DRG=看病不贵?
- 重磅!君实公布首个国产PD
- 枞阳县美好乡村建设摄影大赛二等奖作品
- 全球25大药企排名新鲜出炉,它们的这些进展你都知道吗?
- 索格列净治疗2型糖尿病结果公布 赛诺菲与Lexicon“闹分手”
- 疫苗企业如何在利润与社会责任之间做好平衡与选择
- 搜索